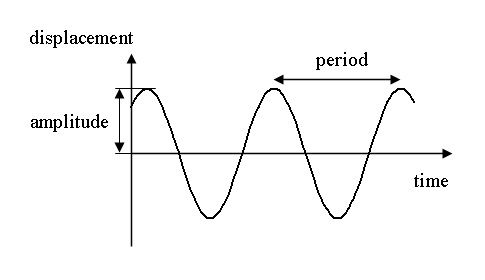
Panjang gelombang dalam fisika dapat diartikan sebagai jarak dari satu puncak ke puncak lainnya disebut jarak panjang gelombang , dan dilambangkan dengan λ. Menurut definisinya, gelombang mengulangi karakteristiknya setelah suatu periode waktu. Sebelum membahas konsep ini, kita harus mengetahui dasar-dasar elektron dan apa itu sebenarnya? Elektron adalah sub partikel dalam atom, dilambangkan dengan “e-”. Elektron ini memiliki muatan listrik negatif. Elektron ini memainkan peran penting dalam transfer listrik menjadi bahan padat. Menurut ilmuwan Prancis Louis de Broglie, elektron juga memiliki sifat gelombang. Dalam tesisnya, ia membuktikan bahwa semua materi / partikel memiliki sifat gelombang bahkan elektron juga. De Broglie mengajukan persamaan untuk mendeskripsikan sifat-sifat materi / partikel. Pada artikel ini de Broglie akan mengetahui panjang gelombang elektron, persamaannya, penurunannya, dan dari Broglie panjang gelombang elektron pada 100 EV .
Berapa Panjang Gelombang Elektron De Broglie?
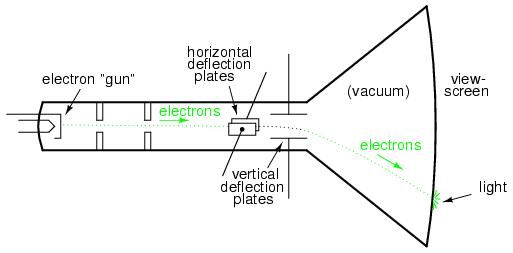
Menurut Louis de Broglie, semua partikel memiliki sifat gelombang. Mereka dapat menunjukkan beberapa properti tipe gelombang. Teori yang sama berlaku untuk elektron juga sesuai pernyataannya.

de-Broglie-panjang gelombang-elektron
Gelombang elektron memiliki panjang gelombang λ dan panjang gelombang ini bergantung pada momentum elektron. Momentum (p) elektron dinyatakan dalam massa elektron (m) dan kecepatan elektron (v).
∴Momentum elektron (p) = m * v
Maka panjang gelombang λ adalah
∴ Panjang gelombang λ = h / p
Di sini h adalah konstanta Planck dan nilainya adalah 6.62607015 × 10-34 J.S
Rumus untuk λ dikenal sebagai panjang gelombang elektron de Broglie. Dengan menganalisis ini kita dapat mengatakan bahwa elektron yang bergerak lambat memiliki panjang gelombang yang besar dan elektron yang bergerak cepat memiliki panjang gelombang yang pendek atau minimum.
De Broglie Panjang Gelombang Penurunan Elektron
Derivasi De Broglie Panjang Gelombang Elektron menyatakan hubungan antara materi dan energi. Untuk menurunkan de Broglie panjang gelombang persamaan elektron , mari kita ambil persamaan energi yaitu
E = m.cdua
Di sini m = massa
E = energi
C = kecepatan cahaya
Dan teori Planck juga menyatakan itu energi kuantum terkait dengan frekuensinya bersama dengan konstanta papan.
E = h.v
∴ Persamaan dua persamaan energi untuk mendapatkan persamaan panjang gelombang de Broglie.
m.cdua= h.v
Partikel nyata apa pun tidak dapat bergerak dengan kecepatan cahaya. Jadi, gantikan kecepatan (v) dengan kecepatan cahaya (c).
m.vdua= h.v
Gantikan 'v' dengan v / λ, lalu m.v2 = h.v / λ
∴ λ = h.v / m.v2a
Persamaan di atas menunjukkan panjang gelombang de Broglie sebuah elektron.
Misalnya, kita dapat menemukan file de Broglie panjang gelombang elektron pada 100 EV adalah dengan mengganti nilai konstanta Planck (h), massa elektron (m), dan kecepatan elektron (v) pada persamaan di atas. Kemudian nilai panjang gelombang de Broglie adalah 1.227 × 10-10m.
Setiap partikel atau materi memiliki sifat tipe gelombang di alam semesta ini menurut de Broglie. Dan mereka bisa memiliki panjang gelombang. Nilai-nilai tersebut dapat diketahui oleh persamaan panjang gelombang de Broglie . Dengan mempertimbangkan kecepatan partikel dan nilai massa serta konstanta Planck kita dapat mengetahui panjang gelombangnya. Partikel yang memiliki nilai massa lebih banyak daripada partikel yang lebih sedikit memiliki panjang gelombang paling kecil.