Sel kering adalah bentuk paling sederhana dari sumber penghasil listrik. Sejumlah sel yang digabungkan menjadi satu membentuk baterai. Itu timbal-asam atau nikel-kadmium baterai adalah versi lanjutan dari sel kering. Sel ini pertama kali ditemukan oleh insinyur Prancis Georges Leclanche pada tahun 1866. Penemuannya dinamai menurut namanya sebagai baterai Leclanche. Tapi saat itu, sangat berat dan mudah pecah. Sel kering memiliki prinsip yang sama dan merupakan versi lanjutan dari baterai Leclanche dan memiliki voltase dan ukuran yang berbeda. Bentuk komersial dari sel seng-karbon yang merupakan bentuk modifikasi dari baterai Leclanche ditemukan pada tahun 1881 oleh Carl Gassner dari Mainz. Ini diproduksi dalam jumlah besar dan digunakan dalam banyak aplikasi seperti mainan, radio, kalkulator, dll.
Apa itu Sel Kering?
Sel kering adalah alat yang menghasilkan listrik berdasarkan reaksi kimia. Ketika dua elektroda sel dihubungkan melalui jalur tertutup, maka sel memaksa elektron mengalir dari satu ujung ke ujung lainnya. Aliran elektron menyebabkan arus mengalir pada rangkaian tertutup.

Lapisan Sel Kering
Dengan bantuan reaksi kimia, elektron mengalir dari satu ujung ke ujung lainnya. Ketika dua atau lebih sel, terhubung dengan polaritas yang benar, lebih banyak elektron mengalir karena potensial tinggi. Kombinasi ini disebut baterai. Dari tegangan minimum 1,5 V hingga 100 V, baterai dapat digunakan untuk mendapatkan kisaran tegangan. Bahkan tegangan DC keluaran baterai dapat diatur ke level yang berbeda menggunakan konverter elektronik daya seperti helikopter sirkuit.
Struktur Sel
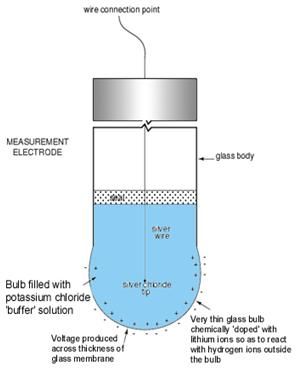
Struktur sel kering seng-karbon ditunjukkan pada gambar. Ini terdiri dari terminal anoda sebagai seng atau batang grafit umum. Karbon membentuk terminal katoda. Dapat diamati bahwa dalam versi sel kering seng digunakan sebagai katoda dan grafit digunakan sebagai terminal anoda. Pemilihan unsur-unsur pada dasarnya didasarkan pada konfigurasi kimianya pada orbit terluar unsur-unsur tersebut.

Struktur Sel Kering
Jika ia memiliki lebih banyak elektron bilangan di orbit terluar, maka ia dapat bertindak sebagai donor, dan karenanya membentuk katoda. Demikian pula, jika orbit terluar memiliki lebih sedikit elektron, ia dapat dengan mudah menerima dan karenanya membentuk anoda. Elektrolit yang ditempatkan di antaranya bertindak sebagai katalisator untuk reaksi kimia. Secara umum, kami menggunakan jeli amonium klorida sebagai elektrolit. Pada gambar yang ditampilkan, elektrolit yang digunakan adalah campuran seng dan klorida. Selain itu, natrium klorida juga digunakan sebagai elektrolit. Campuran mangan dioksida dan karbon dikelilingi di sekitar batang anoda.
Seluruh konfigurasi ditempatkan dalam tabung logam. Agar-agar tidak mengering dengan menggunakan pitch di bagian atas sel. Mesin cuci karbon ditempatkan di bagian bawah. Tujuan dari mesin cuci ini adalah untuk mencegah batang anoda seng bersentuhan dengan wadah.
Ini juga disebut spacer seperti yang ditunjukkan pada diagram. Kaleng seng juga dikelilingi oleh isolasi kertas untuk keperluan isolasi. Untuk baterai besar, bahan isolasi lain seperti mika, dll juga digunakan. Terminal positif el terbentuk di bagian atas. Terminal negatif sel terbentuk di pangkalan.
Pengerjaan Dry Cell
Sel kering pada dasarnya bekerja pada reaksi kimia. Karena reaksi yang terjadi antara elektrolit dan elektroda, elektron mengalir dari satu elektroda ke elektroda lainnya. Zat seperti asam larut dalam air membentuk partikel terionisasi. Partikel terionisasi terdiri dari dua jenis. Ion positif disebut kation dan ion negatif disebut anion. Asam yang larut dalam air disebut elektrolit.
Pada diagram yang disebutkan di atas, seng klorida terbentuk sebagai elektrolit. Demikian pula agar-agar amonium klorida juga terbentuk sebagai elektrolit. Batang logam yang direndam dalam elektrolit membentuk elektroda. Berdasarkan sifat kimiawi dari batang logam tersebut, terdapat elektroda positif sebagai anoda dan elektroda negatif sebagai katoda.
Elektroda menarik ion yang bermuatan berlawanan ke sisinya. Misalnya, katoda menarik anion dan anoda menarik kation. Dalam proses ini elektron mengalir dari satu arah ke arah lainnya, oleh karena itu kita mendapatkan aliran muatan. Ini disebut arus .
Reaksi kimia
Reaksi yang terjadi di dalam sel ditunjukkan di bawah ini. Pertama adalah reaksi oksidasi.

Dalam hal ini, katoda seng dioksidasi menjadi ion seng bermuatan positif yang melepaskan dua ion. Elektron ini dikumpulkan oleh anoda. Kemudian muncul reaksi reduksi.

Reaksi reduksi di anoda ditunjukkan di atas. Reaksi ini menghasilkan arus listrik. Ini melepaskan ion oksida dengan magnesium oksida. Reaksi ini terbentuk ketika magnesium digabungkan dengan elektrolit.


Dua reaksi lainnya merupakan reaksi asam-basa dan reaksi pengendapan yang terjadi di sel kering. Dalam reaksi asam-basa, NH digabungkan dengan OH menghasilkan NH3 bersama dengan air. Hasilnya adalah NH3 dan basis air.
Perbedaan Antara Sel Kering dan Sel Basah
Perbedaan utama antara sel kering dan sel basah adalah bentuk elektrolitnya. Seperti dibahas sebelumnya, dalam sel kering, elektrolit seperti amonium klorida bersifat kering. Sel kering semacam itu lebih umum dan digunakan dalam mainan, radio, dll. Tetapi dalam sel basah, elektrolit dalam keadaan cair.
Elektrolit cair seperti asam sulfat, yang merupakan cairan korosif berbahaya digunakan. Karena sifat cairan tersebut, sel basah lebih mudah meledak dan perlu ditangani dengan hati-hati. Keuntungan terbaik dari sel basah tersebut adalah dapat dengan mudah diisi ulang dan digunakan untuk berbagai aplikasi. Baterai semacam itu umum digunakan dalam penerbangan, utilitas, penyimpanan energi, dan menara telepon seluler.
Fungsi Sel Kering
Fungsi sel kering didasarkan pada reaksi kimia antara elektroda dan elektrolit. Ketika elektroda ditempatkan di elektrolit, itu menarik ion yang bermuatan berlawanan ke arahnya sendiri. Hal ini menyebabkan aliran muatan, dan karenanya arus dihasilkan.
Keuntungan
Itu keuntungan dari sel kering termasuk yang berikut ini.
- Sel kering memiliki banyak keunggulan seperti
- Ukurannya kecil.
- Itu bisa datang dalam berbagai level tegangan.
- Ini berguna dan memiliki banyak aplikasi.
- Ini adalah satu-satunya sumber tegangan DC.
- Ini dapat digunakan bersama dengan sirkuit elektronik daya untuk mengatur tegangan keluaran
- Ini dapat diisi ulang.
Kekurangan
Itu kerugian dari sel kering termasuk yang berikut ini.
- Ini harus ditangani dengan hati-hati
- Itu eksplosif
- Baterai dengan rating besar sangat berat
Aplikasi
Itu aplikasi sel kering termasuk yang berikut ini.
- Mainan
- Penerbangan
- Handphone
- Radio
- Kalkulator
- Jam tangan
- Alat bantu Dengar
Karenanya kami telah melihat operasi, klasifikasi, dan aplikasi file sel kering . Satu hal yang menarik untuk dicatat adalah baterai hanya bekerja ketika elektroda-elektroda tersebut secara fisik bersentuhan satu sama lain. Harus ada media konduktor antara dua elektroda. Pertanyaannya adalah dapatkah air digunakan sebagai media penghantar antara elektroda sel kering? Kalau begitu, apa yang akan terjadi jika sel ini dicelupkan ke dalam air?